近日,中山大学附属第一医院肿瘤内科徐丽霞副教授和精准医学研究院名誉院长于君教授在权威杂志《癌症研究》上发表了一篇名为《N6-甲基腺苷读本YTH DF 1促进干细胞和治疗耐药》的文章。通过增强notch 1表达治疗肝癌的研究论文。
本研究从mRNA m6A修饰的角度出发,深入探讨了YTHDF1读码器在调节HCC干细胞特性和耐药性中的作用和机制。

肝细胞癌(HCC)是最常见的原发性肝癌。其发病隐匿,发现时多为晚期。无法接受手术等根治性治疗,需要靶向药物等系统治疗。索拉非尼和利伐替尼作为晚期肝癌的一线靶向药物,临床有效率不到20%,耐药机制不明。HCC的干细胞在耐药性中发挥着重要作用。因此,寻找抑制LCSCs的有效干预靶点有望从源头上克服HCC的耐药性,对改善患者预后具有重要意义。近年来,研究证实RNA的表观遗传修饰参与许多肿瘤干细胞的功能调节。然而,m6A等mRNA的表观遗传修饰与LCSCs之间的关系尚不清楚。本研究对406例HCC组织和癌旁组织进行了转录组测序,分析了mRNA m6A各种修饰调节因子的表达水平。研究发现,reader YTHDF1在肿瘤组织中的表达显著上调。随后,研究人员检测了来自两个临床队列的肝癌样本中YTHDF1的蛋白表达水平,发现YTHDF1的高表达与HCC患者的不良预后显著相关,并与肿瘤干细胞标志物的上调和靶向药物的耐药性呈正相关。研究人员随后使用HCC器官模型和干细胞特异性转基因小鼠证明YTHDF1显著增强了HCC的干燥程度,并降低了肝癌对靶向治疗药物的敏感性。
在分子机制探索方面,研究人员揭示了YTHDF1通过修饰mRNA m6A与关键干细胞调节因子NOTCH1的mRNA结合,增强NOTCH1的mRNA稳定性和翻译效率,从而提高NOTCH1的表达水平,促进HCC的干燥并诱导HCC对靶向药物的耐药性。研究人员进一步将包裹在纳米脂质体中的YTHDF1-siRNA注射到小鼠体内。结果表明,靶向YTHDF1的纳米脂质体显著抑制了HCC在体内的生长,同时增强了靶向药物索拉非尼和利伐替尼的疗效。
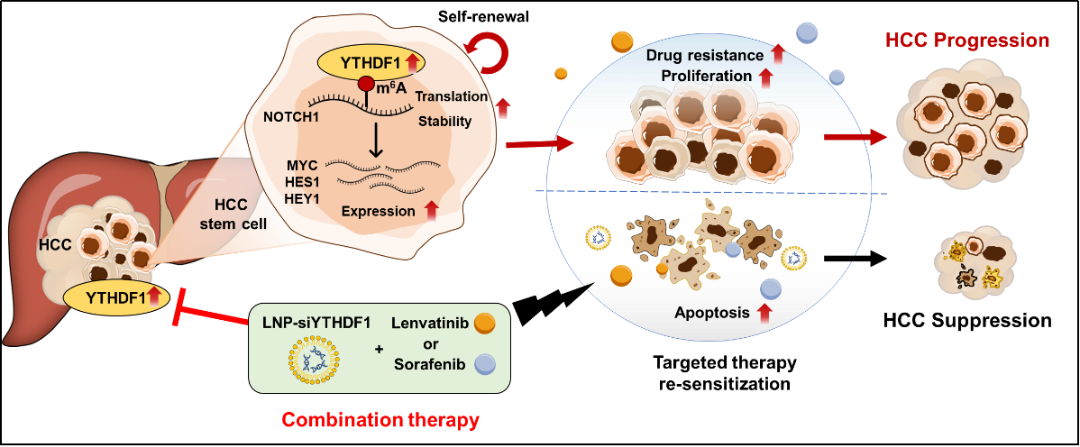
综上所述,该研究揭示了YTHDF1在调节HCC干燥中的重要作用,并阐明了其通过YTHDF1-m6A-NOTCH1表观转录轴促进HCC干燥的新机制,表明YTHDF1有望成为药物治疗的新靶点以敏化HCC。该研究为了解HCC靶向治疗的耐药机制提供了重要线索,并为HCC的药物治疗提供了潜在靶点。
本文是中山一院精准医学研究所与临床科室合作的又一研究成果,有望指导临床实践。中山一院【/br/]
肿瘤科住院医师苏、肿瘤科博士生张馨月、消化内科博士生吴亦凡为第一通讯作者,肿瘤科副教授徐丽霞为最后通讯作者,精准医学研究院名誉院长于君教授为共同通讯作者。
【纸质链接】【/br/]
https://aacrjournals . org/cancer RES/article-abstract/doi/10.1158/0008-5472。甲基腺苷能促进干燥吗?redirected from = full text【/br/]
来源:中山一院【/br/]
校对:、苏【/br/]
一审:张【/br/]
审核:梁佳云【/br/]
终审:彭福祥【/br/]
