慢性阻塞性肺疾病(COPD)是一种严重的肺损伤性疾病,全球患者数以亿计。患有中度或以上疾病的慢性阻塞性肺疾病患者的生活质量会受到严重影响,并且在进展为重度和极重度后,患者往往会因肺结构的大规模损伤而死于呼吸衰竭和心血管并发症。目前慢阻肺的治疗方法主要是减少气流受限,但这些方法主要是对症治疗,不能真正有效地再生和修复受损的肺组织或改善肺通气功能。
针对这一迫切的临床需求,2月14日,同济大学附属东方医院教授团队与广州医科大学附属第一医院钟南山院士、李教授团队和陆军军医大学附属西南医院戴教授团队开展合作。在世界顶级转化医学期刊《科学转化医学》杂志上,发表了“P63+肺祖细胞自体移植治疗慢性目标人群”的文章。疾病治疗(自体P63阳性肺前体细胞移植治疗慢性阻塞性肺疾病)”。
本文报道了P63+ LPC移植在全球开展的一期临床安全性和有效性研究结果,以及相关细胞转录组特征分析,证明P63+ LPC移植具有改善肺通气功能的潜力,为包括慢性阻塞性肺疾病在内的各种重大呼吸系统疾病提供了新的治疗思路。

相当一部分慢性阻塞性肺疾病(COPD)患者,尤其是重度COPD患者,除了气道炎症引起气道重塑外,常伴有肺泡结构破坏,导致肺弥散通气功能下降(DLCO)。DLCO的降低与呼吸困难指数评分、运动能力评估、生活质量评分、急性加重发生率和预期生存期显著相关,是慢性阻塞性肺疾病患者预后的独立预测因子。改善肺通气功能对提高患者生存率具有重要意义。但目前长期吸入支气管扩张剂和糖皮质激素,包括长效抗胆碱能药物、长效β2受体激动剂、吸入糖皮质激素等。,广泛用于慢性阻塞性肺疾病(COPD)稳定期的治疗。大规模临床观察的数据证实,这些药物可以暂时缓解症状,但无法控制COPD患者肺损伤的持续进展和肺功能的持续下降,其延长患者生存期的作用也非常有限。因此,研究人员开始探索基于干细胞的再生医学新方法,以期为慢性阻塞性肺疾病患者提供新的治疗选择。
成人肺中存在多种类型的干细胞和前体细胞,它们在维持肺稳态和修复受损肺组织中发挥着重要作用。其中,以P63、KRT5和SOX9为标志的来自支气管上皮基底层的前体细胞备受关注。这些细胞可以对大规模肺损伤做出反应,并具有分化为各种肺上皮细胞的潜力,这些细胞直接参与肺泡结构的修复和再生。佐为开发了人类P63+ LPC的分离和扩增专利技术R-Clone,发明了LPC的肺移植方法,并在啮齿动物和非人灵长类动物模型中充分验证了细胞移植方法和效果。2016年,课题组与戴团队合作,首次从2例支气管扩张患者体内成功分离扩增自体P63+ LPC,并用于自体肺移植。治疗半年后,观察到良好的安全性和肺功能的显著改善(Ma,protein & amp;Cell,2018等。).上述研究背景为后续更大规模、更高水平的临床研究奠定了基础。
这是来自支气管上皮基底层的P63+ LPC。
临床治疗过程
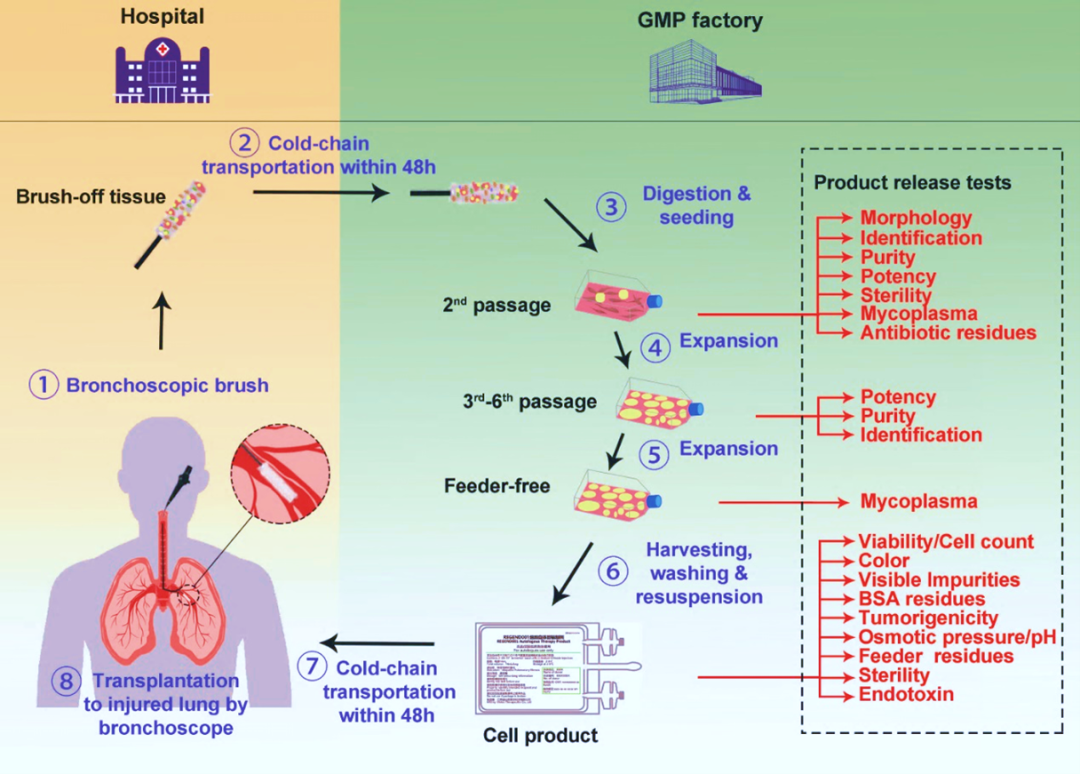
本研究报告了一项为期6年、由研究人员发起、开放标签和对照的临床研究,旨在评估自体P63+ LPC移植治疗慢性阻塞性肺疾病的安全性和治疗效果。受试者为根据COPD全球诊断标准(GOLD)处于II-IV期的COPD患者和弥散功能指数(DLCO)低于80%的患者,其中大多数为重度或极重度COPD患者。共有20名受试者完成了试验和随访,包括3名接受标准治疗(SOC)的对照受试者和17名接受标准治疗+细胞治疗的受试者。两组之间的基线数据没有统计学差异。其中,治疗组的P63+ LPC通过空气刷洗取样,在集美盛瑞GMP车间通过R-Clone专利系统培养和扩增,最后通过纤维支气管镜以0.7~5.2x106细胞/Kg体重的剂量移植到患者自身肺中。
安全方面
细胞治疗组的整体表现良好。在基线、细胞移植后3天、4周、12周和24周随访患者以收集安全性信息。在4周、12周和24周后,在任何患者组的胸部连续CT扫描中都没有发现新的病理或肿瘤形成的迹象。随访期间,对照组和细胞治疗组共出现24例不良事件(AE),未出现严重不良事件(SAE)。其中16例AE为支气管镜检查相关的一过性不良事件,包括恶心、痰中带血和呼吸困难。细胞剂量与不良事件的频率和严重程度之间没有相关性。
就疗效评估而言
本研究以一氧化碳弥散量(DLCO)占预测值的百分比作为主要疗效评价指标,用于评价患者治疗前后肺通气功能的变化。细胞治疗组的受试者在DLCO指数方面表现出明显的改善(24周时与基线相比的DLCO变化:+18.2%),与对照组相比具有统计学意义(24周时与基线相比的DLCO变化:-17.4%)(p值=0.008)。经过12周的细胞治疗后,患者自身也表现出统计学上的显著差异,细胞治疗组中高达70.6%的受试者将DLCO改善至临床获益水平。此外,细胞治疗组受试者的运动能力(6分钟步行距离)和生活质量(SGRQ问卷)的改善趋势也优于对照组,其中66.7%的受试者的6分钟步行距离增加了30米以上,而对照组没有人达到这一标准,显示出显著的统计学差异(p值=0.036)。值得注意的是,对于微肺气肿类型的慢性阻塞性肺疾病患者,可以通过细胞治疗后的CT图像观察肺气肿面积的减少。此外,通过对不同供体细胞的转录组进行测序,发现与对治疗无反应的受试者相比,对治疗有反应的受试者的LPC细胞表达更高水平的P63和更低水平的炎症相关因子。这表明未来经过自体细胞的进一步筛选和转化,有望进一步提高治疗水平。
综上所述,该研究是全球首个正式发表的基于肺再生机制的细胞治疗临床试验,并观察到P63+ LPC细胞治疗显示出远超传统标准治疗方法的慢阻肺治疗潜力。该试验的成功为慢阻肺的治疗提供了一种全新的策略,有望为全球数亿慢阻肺患者带来更有效的治疗选择。2023年9月,佐为教授在业内权威的ERS会议上首次报告了该研究的数据结果,引起了整个呼吸领域的高度关注,并将其结果选为会议年度最重要的三项进展之一,并在官方新闻发布会上向全球媒体发布。目前,这种前体细胞疗法已于2020年在国家医药产品管理局获得药物临床试验默示许可,并分别用于慢性阻塞性肺疾病II期(CXSL2100091)和特发性肺纤维化I/II期(CXSL900019)的注册临床试验,以进一步评估自体P63+ LPC肺内移植的安全性和有效性。
同济大学附属东方医院是本研究的第一交流单位。同济大学附属东方医院的佐为教授、广州医科大学附属第一医院的钟南山院士和李教授以及陆军军医大学西南医院的戴教授是论文的共同作者。同济大学医学院助理研究员博士、南京医科大学附属淮安市第一人民医院孟教授/主任医师、广州医科大学附属第一医院刘明副主任医师、吉美瑞上海超级器官研发中心周月清博士和广州医科大学附属第一医院陈迪飞博士是本研究的共同第一作者。另一位资深作者张婷博士也为这项研究做出了重要贡献。Regend Therapeutics作为项目发起人,为该项目提供了主要研究资金。此外,项目团队获得了国家重点研发计划干细胞项目、国家自然科学基金项目、国家生物技术药物创新中心“揭榜”项目和江苏省重点研发计划的部分支持。
原始链接
https://www.science.org/doi/10.1126/scitranslmed.adi3360
来源:同济大学医学院佐为教授。
