近日,重庆医科大学唐霓/汪凯/黄爱龙团队在国际知名期刊《Journal of Clinical Investigation》上发表了题为“Gluconeogenic enzyme PCK1 supports S-adenosylmethionine biosynthesis and promotes H3K9me3 modification to suppress hepatocellular carcinoma progression”的研究论文。该研究发现糖异生酶 PCK1 通过丝氨酸合成途径促进 S-腺苷甲硫氨酸 (SAM) 的生成。甲基转移酶 SUV39H1 催化 SAM 作为甲基供体支持 H3K9me3 修饰,从而抑制癌基因 S100A11。

https://www.jci.org/articles/view/161713
01 研究背景
表观遗传学的改变和基因表达模式的异常是癌症的主要特征。组蛋白的翻译后修饰失调(PTMs),如甲基化和乙酰化,被认为在许多癌症的发生和发展中起着重要作用。
组蛋白甲基化是由组蛋白甲基转移酶(HMT)催化的,它可以激活或抑制基因表达,这取决于被修饰的特定组蛋白残基以及添加的甲基数量。研究最广泛的组蛋白甲基化位点,包括H3K4,H3K36和H3K79通常与转录激活有关,而H3K9me2、H3K9me3和H3K27me3作为抑制标记。
HMT使用s -腺苷蛋氨酸(SAM)作为甲基供体,将其甲基转移生成s -腺苷同型半胱氨酸(SAH)和甲基化底物。
SAM是通过蛋氨酸腺苷转移酶从蛋氨酸循环中产生的。细胞SAM浓度与酶Km值(甲基转移酶反应半最大速度(½Vmax)时SAM浓度)相称(10,11),甲基化状态的变化是由于hmt酶活性的差异而发生的。
因此,组蛋白甲基化状态可能受到SAM或SAM合成调节因子波动的影响,将代谢与表观遗传调节联系起来。最近的研究表明,肝脏可以被认为是人体的SAM工厂,近85%的甲基化反应发生在肝脏,这表明异常的SAM水平或异常的组蛋白甲基化可能在癌症的发生中起重要作用。
糖异生是糖酵解的逆向途径,主要发生在肝脏,在代谢重编程和肿瘤生长中起关键作用。胞质异构体 PCK1 (也称为 PEPCK-C 或 PEPCK1) 是肝脏糖异生的初始酶,催化草酰乙酸 (OAA) 转化为磷酸烯醇丙酮酸 (PEP)。既往研究发现,PCK1 在肝细胞癌 (HCC) 中下调,敲除 PCK1 可增强肝癌在体内和体外的增殖和转移。然而,PCK1 在 HCC 中的复杂代谢功能和机制尚未明确,PCK1 是否在组蛋白甲基化中发挥代谢作用以控制基因表达仍不清楚。
02 研究发现
本研究结果表明,通过增强S100A11启动子的H3K9me3修饰和下调PI3K/AKT信号通路,依赖pck1的SAM的产生对HCC抑制很重要。先前的研究表明,PCK1表达升高导致激活p-AMPK的细胞ATP水平降低,而PCK1的缺失导致核糖-5-磷酸(R5P)的积累,从而保护细胞免受氧化损伤,并增强UDP-GlcNAc的生物合成,从而上调o - glcn酰化。此外,最近一项关于T细胞记忆稳态的研究发现,PCK1通过糖异生途径促进G6P和R5P的生物合成,从而确保ROS的猝灭,促进CD8+ Tm细胞的存活。
然而,研究表明PCK1驱动TCA中间体进入SSP,维持相对较高的SAM水平。SAM水平升高通过甲基转移酶SUV39H1增强H3K9me3组蛋白甲基化,从而抑制致癌基因S100A11的转录和表达。PCK1的缺失导致S100A11的增强,S100A11招募AKT1促进PI3K/AKT信号通路,从而促进肿瘤进展。这些发现阐述了PCK1在HCC中的潜在调控机制,并提供了SAM水平波动如何调节特定基因表达的见解。这些结果强调了代谢重编程和表观遗传修饰之间的关联,以更有效地治疗HCC。
最近的研究表明,SAM补充剂可以通过引起高甲基化介导的前转移基因失活来抑制细胞增殖和侵袭。
另外本研究还证明了S100A11直接与AKT1相互作用,激活PI3K/AKT信号,启动HCC中的增殖和迁移。
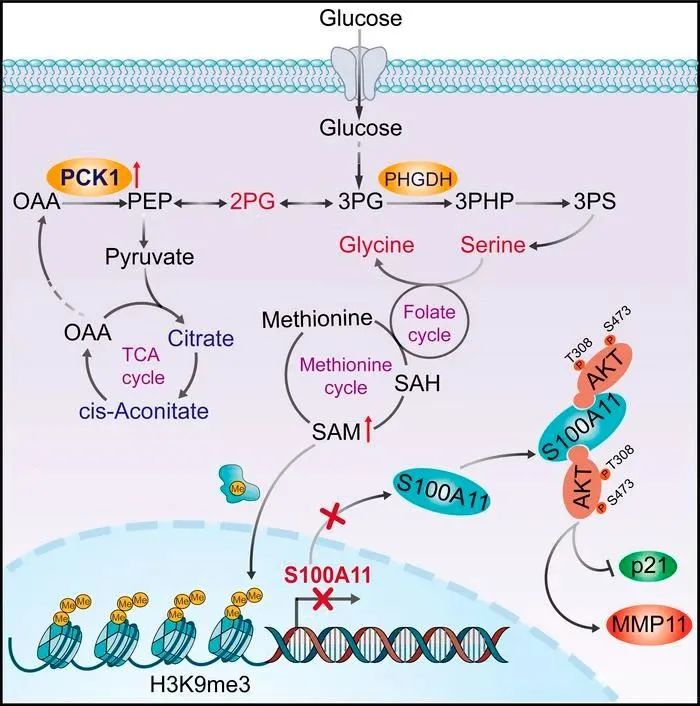
PCK1调节表观遗传调控示意图
03 研究意义
综上所述,PCK1的低表达主要通过限制SAM的生成来降低H3K9me3修饰,从而增强S100A11的转录和表达以及PI3K/AKT通路的异常激活,从而促进HCC的恶性发展和进展。这些发现为pck1介导的组蛋白甲基化在肿瘤抑制中的作用和贡献提供了见解,这意味着代谢的波动与表观遗传修饰的失调密切相关。因此,靶向这些途径获得SAM和抑制癌基因S100A11在HCC的临床治疗中具有潜在的应用前景。
参考资料:https://www.jci.org/articles/view/161713
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
